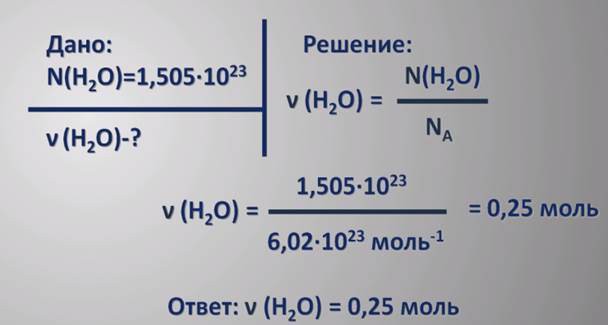
現代化学におけるOVRとは何ですか?
無機および有機合成のOVRについて教えてください。
プロセス定義
レドックス反応には、複雑なまたは単純な物質中の2つ以上の化学元素の酸化の程度の変化をもたらすプロセスが含まれる。

酸化とは何ですか?
酸化とは、そのような化学物質原子または特定のイオンが電子を放出し、その初期の酸化状態を低下させる反応。このプロセスは金属に特有のものです。
回復とは何ですか?
修復のプロセスとは電子の添加によって、イオンまたは単体物質中の酸化の程度が減少することになる。この反応は、非金属および酸残留物に特徴的である。

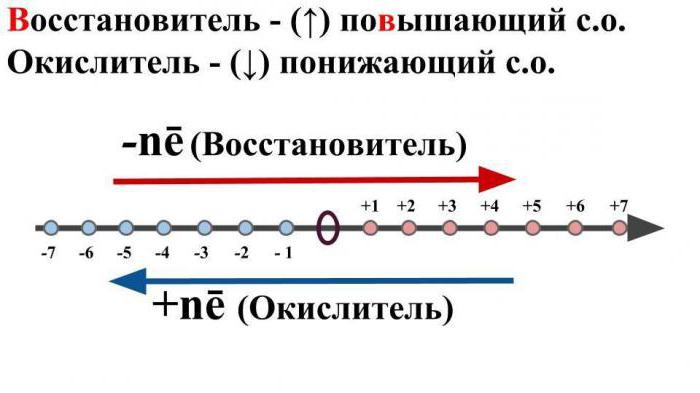
還元剤の特性
OVRとは何かという問題を考えると、「還元剤」という概念を無視することはできません。
それは、中性分子または化学的相互作用の結果として、その酸化度を増加させながら他のイオンまたは原子電子を与える。

酸化剤の測定
OVRとは何かを疑うことも重要です「酸化剤」のような用語も言及する。これにより、化学的相互作用の間に他の原子または中性粒子から負の電子を取り出すようなイオンまたは中性原子を意味することが通例である。同時に、その初期の酸化状態が低下する。
OBRの種類
OVRとは何かを考えて、無機および有機合成で最も頻繁に考えられるこれらのプロセスの種類について注意する必要があります。
分子間相互作用は、還元剤と酸化剤の両方の原子が、相互作用に入る異なる出発物質に位置する方法。この種の変換の例は、酸化マンガン(4)と塩酸との相互作用であり、これはガス状の塩素、二価の塩化マンガン、および水をもたらす。
この化学プロセスでは、塩素アニオンは相互作用すると酸化するように見える。マンガンのカチオン(酸化状態+4)は、2つの電子を取って反応中の酸化能力を示し、回復する。
分子内相互作用は、そのような化学変換は、還元剤の原子と酸化剤の原子の両方が最初に1つの源物質であり、変換の完了後にそれらは様々な反応生成物中に存在する。
このタイプの反応の一例として、塩素酸カリウムの分解を表す。加熱すると、この物質は塩化カリウムと酸素に変わる。酸化特性は塩素酸アニオンに特徴的であり、反応中の5電子をとると塩化物に還元される。
この場合、酸素アニオンが現れる分子酸素に酸化されて還元される。この場合、OVRとは何ですか?これは、イオン間の電子の移動のプロセスであり、2つの反応生成物の形成をもたらす。
このタイプの化学変換にも、最初に1つの式で見いだされた元素の酸化度の変化に伴って起こる反応は、亜硝酸アンモニウムの分解プロセスである。プロセス中に酸化度が-3であるアンモニウムカチオン中に立っている窒素は、6電子を与え、分子状窒素に酸化される。亜硝酸塩の一部である窒素は還元剤であるが、6電子を取り、反応中は酸化される。
化学におけるOVRとは何ですか?上記の定義は、これらが酸化状態のいくつかの要素の変化に関連する変換であることを示している。
自己酸化および還元(不均衡)還元剤および酸化剤として、その過程で増加し、同時に相互作用の完了後にその酸化状態を減少させる1つの初期原子が存在すると仮定する。化学におけるOVRとは何かを考えて、そのような変容の例は中等学校の化学の過程でも見いだされる。加熱時の亜硫酸カリウムの分解は、この金属の2つの塩、すなわち硫化物および硫酸塩の形成をもたらす。 +4の酸化状態を有する硫黄は還元性および酸化性の両方を示し、酸化状態を増減させる。
OVIが化学で何を意味するのかを理解するために、それをそのような化学変換の別のタイプ。対比はそのようなプロセスを含み、その結果、還元剤および酸化剤の原子は異なる初期成分の組成にあるが、右側ではそれらは1つの反応生成物を形成する。例えば、硫黄酸化物(4)と硫化水素との相互作用において、硫黄および水が形成される。酸化状態が+4の硫黄イオンは4電子、指数-2の硫黄イオンは2電子を失う。結果として、それらは両方とも、酸化の程度がゼロである単純な物質に変わる。

結論
化学におけるOVRが何であるかの問題を考えると、我々はこれらが多数の形質転換であり、それを通して生きている生物が機能し、様々な自然のプロセスと現象が起こることに気付く。このような方程式に係数を配置するには、電子天びんをコンパイルする必要があります。