アボガドロの番号:興味深い情報
学校の化学科目からわかるように、もしある種の物質を1モルとすると、6.02214084(18)・10 ^ 23原子または他の構造要素(分子、イオンなど)が存在します。便宜上、Avogadroの番号は通常6.02?10 ^ 23の形式で書かれています。

正確に言えば、Amedeo Avogadroは、一定量の分子や原子の計算を扱っていませんでした。どのくらい多くの分子のガスを見つけるか最初に試みる

その後、多数のアボガドロの数を決定する方法の独立した方法であり、その結果はほとんど一致したので、これは分子の実際の存在に賛成しています。現時点では、方法の数は60を超えていますが、近年、科学者は「キログラム」という用語の新しい定義を導入するために評価の精度をさらに向上させようとしています。今のところ、キログラムは基本的な定義なしに選択された材料規格と比較されます。
しかし、私たちの質問に戻りましょう。なぜこの定数は6.022?10 ^ 23ですか?

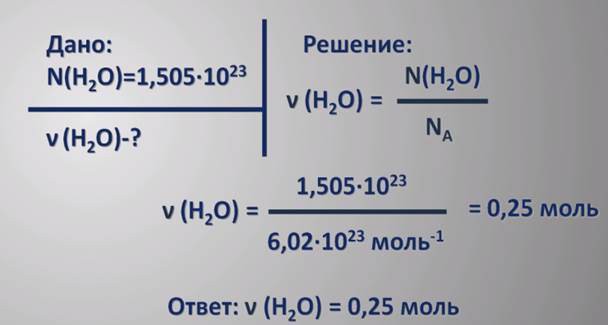
わかりやすくするために、例を挙げてみましょう。 原子質量単位の定義からわかるように、1amu。 12Cの1つの炭素原子の12分の1に相当し、1.66053878・10 ^(-24)グラムである。 1 amuを掛ければアボガドロの定数では、それは1.000 g / molになります。今、ベリリウムのような化学元素を取ります。この表によれば、1つのベリリウム原子の質量は9.01amuである。この元素の1モルの原子を数えましょう:
6.02×10 ^ 23モル-1×1.66053878×10 ^(-24)グラム×9.01 = 9.01g /モル。
したがって、モル質量は原子質量と数値的に一致することが分かる。
恒久的なアボガドロは特別に選ばれたので、モル質量が原子または次元のない値、すなわち相対分子(原子)質量に対応するようにする。アボガドロの数は、一方では質量の原子単位に、他方では質量グラムを比較するための共通単位に現れると言えます。